Abstract
Contexte: Le rôle du remdésivir dans le traitement des patients hospitalisés pour la COVID-19 reste imprécis dans un contexte international. L’essai randomisé et contrôlé (ERC) Solidarity de l’Organisation mondiale de la Santé a évalué le remdésivir chez des patients de nombreux pays; le Canada a inscrit des patients dans un protocole élargi de collecte de données: l’essai CATCO (Canadian Treatments for COVID-19). Nous faisons état des observations canadiennes, des données démographiques, des caractéristiques et des indicateurs cliniques qui témoignent de la variabilité des effets d’un système de santé à l’autre.
Méthodes: Nous avons procédé à un ERC pragmatique à étiquetage en clair dans les hôpitaux canadiens, en collaboration avec l’essai Solidarity. Nous avons procédé à une attribution aléatoire des patients à 10 jours au remdésivir (200 mg par voie intraveineuse [IV] au jour 0, suivis de 100 mg IV par jour) en plus du traitement standard, ou au traitement standard seulement. L’indicateur principal était la mortalité perhospitalière. Les indicateurs secondaires incluaient les modifications de la gravité de l’état clinique, le nombre de jours sans oxygénothérapie et sans ventilation (à 28 jours), l’incidence d’un nouveau recours à l’oxygénothérapie et à la ventilation mécanique, la durée du séjour hospitalier et les taux d’effets indésirables. Nous avons effectué des analyses de sous-groupes préspécifiés selon la durée des symptômes avant le recrutement, l’âge, le sexe, et la gravité des symptômes à l’arrivée.
Résultats: Parmi 52 hôpitaux canadiens, entre le 14 août 2020 et le 1er avril 2021, nous avons procédé à une attribution aléatoire de 1282 patients au remdésivir (n = 634) ou au traitement standard (n = 648). Parmi ces patients, 15 ont retiré leur consentement ou étaient encore hospitalisés, pour un échantillon total de 1267 patients. Parmi les patients auxquels on a attribué le remdésivir, la mortalité perhospitalière a été de 18,7 %, contre 22,6 % chez les patients sous traitement standard (risque relatif [RR] 0,83, intervalle de confiance [IC] de 95 % 0,67–1,03 et la mortalité à 60 jours a été de 24,8 % et 28,2 %, respectivement (IC de 95 % 0,72–1,07). Pour les patients non ventilés mécaniquement au départ; le recours à la ventilation mécanique a été de 8,0 % chez les patients qui recevaient le remdésivir et de 15,0 % chez ceux sous traitement standard (RR 0,53, IC de 95 % 0,38–0,75). Le nombre moyen de jours sans oxygénothérapie ni ventilation au jour 28 étaient de 15,9 (± écart-type [É.T.] 10,5) et 21,4 (± É.-T. 11,3) chez les patients sous remdésivir et de 14,2 (± É.-T. 11) et 19,5 (± É.-T. 12,3) chez les patients sous traitement standard (p = 0,006 et 0,007, respectivement). On n’a noté aucune différence quant à l’innocuité (p. ex., recours à la dialyse, changement du taux de créatinine, ou nouveaux cas d’insuffisance hépatique) entre les 2 groupes.
Interprétation: Comparativement au traitement standard, le remdésivir a eu un effet modeste, mais significatif sur certains indicateurs importants pour les patients et pour les systèmes de santé, tels que le recours à la ventilation mécanique.
Numéro d’enregistrement de la recherche: ClinicalTrials.gov, no. NCT04330690.
Le rôle du remdésivir dans le traitement des patients hospitalisés pour la COVID-19 reste imprécis1. Le remdésivir, un antiviral « adapté », a été approuvé entièrement ou en situation d’urgence par de nombreux organismes de réglementation, y compris par Santé Canada, pour le traitement de la COVID-19, sur la base de données d’essais cliniques faisant état d’un rétablissement plus rapide2. Un rapport provisoire du volumineux essai Solidarity de l’Organisation mondiale de la Santé (OMS) n’a montré aucune différence au plan de la mortalité ou du recours à la ventilation mécanique, et plusieurs petits essais ont été non concluants pour ce qui est de ces importants indicateurs3–6. Les recommandations des lignes directrices cliniques sont mitigées. Certaines recommandent le remdésivir comme traitement standard et d’autres le déconseillent faiblement7,8. Son incidence sur d’autres indicateurs cliniques, y compris sur l’utilisation des ressources et certains indicateurs post-hospitaliers, n’a pas été clairement définie et l’effet du traitement pourrait être important, particulièrement chez certains groupes de patients9.
L’essai Solidarity est un essai clinique pragmatique international qui mesure les effets de différents traitements sur les patients atteints de COVID-193,10. L’essai CATCO (Canadian Treatments for COVID-19) est une sous-étude de Solidarity subventionnée par les Instituts de recherche en santé du Canada (IRSC) au cours de laquelle d’autres éléments sont recueillis pour mieux comprendre les effets de certains agents spécifiques. Nous avons voulu comparer les effets du remdésivir et du traitement standard chez les patients hospitalisés pour la COVID-19 au Canada; des données internationales, incluant des patients canadiens répartis aléatoirement avant le 29 janvier 2021, seront aussi accessibles dans une publication distincte.
Méthodes
L’essai CATCO est un essai randomisé et contrôlé (ERC) multicentrique pragmatique à étiquetage en clair au cours duquel plusieurs agents sont comparés au traitement standard actuellement disponible. Les patients admissibles sont des adultes porteurs d’une infection au SRAS-CoV-2 confirmée en laboratoire, admis dans les hôpitaux participants (annexe 1, accessible en anglais ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211698/tab-related-content). Les critères d’exclusion étaient allergie au médicament de l’étude, transfert prévu vers un site non participant, survie prévisible de moins de 24 heures ou patient déjà sous remdésivir au moment du recrutement. L’insuffisance rénale ou hépatique au départ n’était pas un critère d’exclusion spécifique. L’effet d’autres médicaments étudiés dans l’essai CATCO, comme l’interféron, l’association lopinavir–ritonavir et l’hydroxychloroquine, a fait l’objet d’un rapport provisoire précédent de l’étude Solidarity3.
Nous avons procédé à une attribution aléatoire des patients admissibles ayant donné leur consentement, soit au schéma thérapeutique interventionnel remdésivir (intraveineux [IV]) 200 mg au jour 0, puis 100 mg aux jours 1 à 9 plus traitement standard, soit au traitement standard seulement (groupe témoin). Toutes les autres décisions en matière de soins relevaient des médecins traitants, y compris les traitements d’appoint, comme la dexaméthasone ou le tocilizumab ou une association des deux, chez les patients admissibles, selon la période, le contexte hospitalier et la participation à d’autres ERC11. Les patients recevaient leur congé lorsque l’équipe soignante les jugeait cliniquement prêts et l’intervention étudiée était cessée si le congé survenait avant l’administration d’un cycle thérapeutique complet. Le consentement était obtenu soit a priori, soit plus tard, selon les exigences des comités d’éthique locaux. Nous avons procédé à une randomisation non stratifiée, selon un rapport 1:1. Après le rapport d’analyse provisoire initial de Solidarity, le recrutement a privilégié les patients qui n’étaient pas sous ventilation mécanique3. Nous avons procédé à la randomisation par l’entremise de l’essai international Solidarity jusqu’au 29 janvier 2021, et au Canada, jusqu’au 1er avril 2021, avec l’aide d’un serveur Web après l’arrêt de la randomisation au remdésivir de l’essai Solidarity. À cet égard, l’essai CATCO a recruté plus de patients canadiens que dans l’essai international Solidarity, utilisant tous les mêmes rapports de répartition aléatoire non stratifiés.
Indicateurs de résultats
Le principal indicateur de l’essai international Solidarity était la mortalité perhospitalière et les indicateurs secondaires étaient un nouveau recours à la ventilation mécanique (pour les individus non ventilés au départ) et la durée du séjour hospitalier3. Les autres indicateurs secondaires prédéfinis pour l’essai CATCO inclus dans ce rapport étaient la gravité clinique de la maladie aux jours 3, 5, 8, 11, 15, 29 et 60 (y compris après le congé), selon l’échelle ordinale de l’OMS12; les nombres de jours sans oxygénothérapie et sans ventilation au jour 28 suivant la randomisation, correspondant respectivement à 0 si le patient était décédé dans les 28 jours, et à 28 moins le nombre de jours sous oxygénothérapie ou sous ventilation13; et des indicateurs d’innocuité d’intérêt spécial, tels qu’une nouvelle insuffisance hépatique et un nouveau recours à un traitement de remplacement rénal. Nous n’avons pas effectué d’analyses exploratoires préspécifiées sur la proportion de patients ayant obtenu des frottis viraux négatifs à divers moments après la randomisation, compte tenu du manque de données à cet égard.
Analyse statistique
En ce qui concerne les patients de l’essai CATCO, nous faisons état de l’indicateur principal et des 2 indicateurs secondaires de l’essai Solidarity, en plus des indicateurs secondaires mentionnés plus haut. L’analyse primaire était basée sur l’intention de traiter. Nous rapportons la mortalité de toutes causes et les indicateurs secondaires binaires sous forme de proportions, risques relatifs, différences des risques absolus et intervalles de confiance (IC) de 95 %. Nous avons analysé les indicateurs secondaires de gravité clinique à l’aide d’un modèle de risques proportionnels, en tenant compte de la gravité des symptômes à l’arrivée selon la position sur l’échelle ordinale au départ. L’hypothèse de proportionnalité pour les indicateurs de gravité clinique ne s’est pas vérifiée pour certains indicateurs et nous avons donc comparé les groupes avec le test de la somme des rangs de Wilcoxon. Nous avons utilisé le modèle de Fine et Gray pour comparer l’intervalle avant le congé de patients vivants en tenant compte du risque de mortalité concurrent et nous présentons les résultats pour la fonction de risque de sous-répartition et les IC de 95 %. Nous résumons la durée des séjours hospitaliers et les jours sans oxygénothérapie et sans ventilation sous forme de moyennes et d’écarts-types (É.-T.), et de médianes et d’écarts interquartiles (ÉI); les différences entre les groupes pour les médianes et les IC de 95 % se fondent sur la méthode Hodges–Lehman. Les analyses de sous-groupes pour l’indicateur principal de mortalité évaluaient l’effet du traitement entre les sous-groupes préspécifiés suivants avec tests d’interaction: durée des symptômes avant le recrutement (< 7 j), âge inférieur à 55 ans, sexe, et gravité des symptômes à l’arrivée (définie par le degré d’assistance respiratoire, y compris oxygénothérapie de bas débit, oxygénothérapie par voie nasale à haut débit, ventilation non effractive et ventilation mécanique effractive). Aucune imputation n’a été faite pour les données manquantes. Étant donné que cette étude faisait partie d’un essai international adaptatif, nous n’avons pas effectué de calculs relatifs à sa puissance statistique. Les valeurs p inférieures à 0,05 dénotent une portée statistique pour les indicateurs primaire et secondaires qui n’ont pas été ajustés en fonction de la multiplicité. Nous avons effectué toutes les analyses statistiques avec le logiciel SAS (version 9,4, Cary, NC).
Approbation éthique
Cette étude a été approuvée par les comités locaux d’éthique de la recherche, et coordonnée par l’Institut de recherche Sunnybrook. L’essai a été réalisé selon les principes des Lignes directrices de bonne pratique clinique du Conseil international sur l’harmonisation (http://www.ich.org).
Résultats
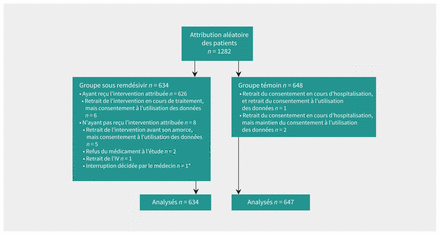
Entre le 14 août 2020 et le 1er avril 2021, nous avons procédé à une attribution aléatoire de 1282 patients soit au remdésivir (n = 634) soit au traitement standard (n = 648) (figure 1) dans 52 hôpitaux canadiens (annexe 1, tableau S2). Parmi eux, des données sur les indicateurs étaient manquantes pour 15 patients (9 ayant retiré leur consentement et 6 étant encore hospitalisés au moment de l’analyse), ce qui donne un échantillon total de 1267 pour l’indicateur principal de mortalité. Cet article inclut 951 patients qui seront intégrés dans le rapport de l’essai international Solidarity.
Diagramme montrant le recrutement, la randomisation et l’inclusion des patients dans les analyses. Remarque: IV = intraveineux. *Un patient avait 2 motifs de retrait.
Caractéristiques de départ
Le tableau 1 montre les caractéristiques des patients au départ. Fidèle au profil démographique des patients hospitalisés durant cette pandémie au Canada, on note une proportion appréciable de personnes racialisées et présentant des comorbidités préexistantes. L’utilisation de la corticothérapie au départ, qui était le traitement standard pour les patients hospitalisés sous oxygénothérapie pendant la majeure partie de cette période de l’essai, était similaire entre les groupes. Le traitement par tocilizumab a été faible (1,5 %), ce qui concorde avec l’évolution des modes de pratique dans les hôpitaux canadiens. La plupart des patients étaient sous oxygénothérapie à faible débit (54,5 %) au jour 1, et 21,4 % étaient hospitalisés dans une unité de soins intensifs (USI) au moment de la randomisation. Cinquante-sept (57) travailleurs de la santé et 1 patiente enceinte faisaient partie de l’essai.
Caractéristiques des patients au départ lors de l’essai CATCO
Indicateurs de résultats
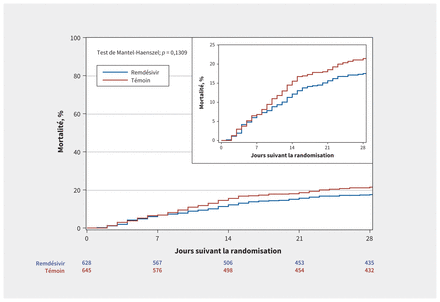
Parmi les patients auxquels on a attribué le remdésivir, la mortalité perhospitalière a été de 18,7 %, contre 22,6 % chez les patients soumis au traitement standard (risque relatif [RR] 0,83, IC de 95 % 0,67–1,03) (annexe 1, figure supplémentaire S1 et tableau supplémentaire S3), et la mortalité à 60 jours a été de 24,8 % et 28,2 %, respectivement (RR 0,88, IC de 95 % 0,72–1,07). Pour les patients qui n’étaient pas sous ventilation mécanique au départ, le recours à la ventilation mécanique a été de 8,0 % chez ceux qui recevaient le remdésivir et de 15,0 % chez ceux qui recevaient le traitement standard (RR 0,53, IC de 95 % 0,38–0,75). Le nombre moyen de jours sans oxygénothérapie et sans ventilation au jour 28 était de 15,9 (± É.-T. 10,5) et 21,4 (± É.-T. 11,3) chez ceux qui recevaient le remdésivir et de 14,2 (± É.-T. 11) et 19,5 (± É.-T. 12,3) chez ceux qui recevaient le traitement standard (p = 0,006 et 0,007, respectivement). La durée des séjours hospitaliers n’a pas différé entre les 2 groupes (médiane 10 [ÉI 6–18] dans le groupe sous remdésivir c. 9 [ÉI 6–17] dans le groupe témoin) (figure 2), et nous n’avons observé aucune différence quant à la durée du séjour hospitalier chez les survivants (tableau 2).
Intervalle entre randomisation et mortalité: données censurées à partir du congé hospitalier, 15 ou 29 j, selon la dernière observation. Remarque: IC = intervalle de confiance, RR = risque relatif.
Indicateurs cliniques des patients de l’essai CATCO
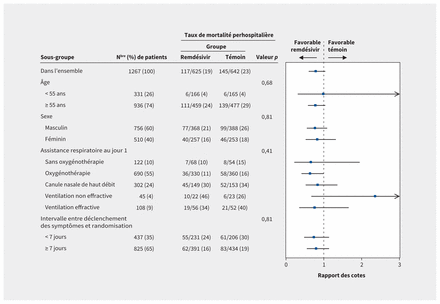
L’examen de la mortalité perhospitalière dans les sousgroupes préspécifiés montre que l’effet du traitement n’a pas varié selon l’âge, le sexe, la gravité de la maladie ou la durée des symptômes (figure 3).
Diagramme en forêt des sous-groupes pertinents. Remarque: La valeur p provient du test d’interaction entre le traitement et n’importe quelle variable des sous-groupes.
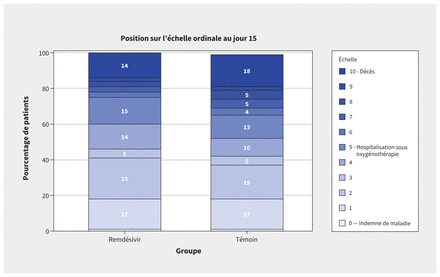
Le rétablissement clinique, selon la position à l’échelle ordinale de l’OMS, est présenté au tableau 3 et le statut au jour 15, à la figure 4.
État clinique à l’échelle ordinale en 10 points de l’Organisation mondiale de la Santé avec le remdésivir c. Tx standard dans un modèle de risques proportionnels ajusté en fonction de la position à l’échelle ordinale au jour 1*
Gravité de l’état clinique selon la position sur l’échelle ordinale de l’Organisation mondiale de la Santé 15 jours après la randomisation (de 0 à 10, 10 correspondant au décès).
Innocuité
On n’a noté aucune différence quant aux indicateurs secondaires d’innocuité entre les groupes soumis à l’intervention pour ce qui est de la créatinine sérique au jour 5, et de l’incidence des nouvelles dialyses ou de l’insuffisance hépatique (tableau 2).
Interprétation
Dans le volet CATCO de l’essai clinique international Solidarity de l’OMS, nous avons constaté que sur 1282 patients admis pour la COVID-19 dans 52 hôpitaux au Canada, la mortalité perhospitalière des patients traités par remdésivir a été moins élevée que celle du groupe témoin. Les petits essais régionaux risquent fort d’être dotés d’une puissance statistique insuffisante pour détecter les effets modestes, mais importants du traitement et la collaboration internationale est fondamentale. Pendant ce temps, comprendre le rôle des traitements dans différents systèmes de santé requiert une analyse soigneuse des données pour détecter les effets régionaux et comprendre si certaines différences sont l’effet du hasard14.
Dans un éventail de sous-groupes préspécifiés de patients établis selon l’âge, le sexe, le degré d’assistance respiratoire à l’admission, et la durée des symptômes, le risque de mortalité perhospitalière a concordé avec les principales observations concernant l’ensemble des patients canadiens (figure 3). Le bienfait du traitement a été le plus manifeste sur le plan de la prévention du recours à la ventilation mécanique, ce qui suggère une valeur ajoutée probable pour les patients moins gravement atteints afin d’éviter la détérioration de leur état durant le séjour hospitalier. Nous avons constaté un plus grand nombre de jours sans ventilation ni oxygénothérapie chez les patients sous remdésivir, de même qu’une amélioration du rétablissement clinique au jour 15, qui concordent en majeure partie avec d’autres essais publiés, y compris l’essai ACTT-1 (Adaptive COVID-19 Treatment Trial), réalisé par Wang et coll., et l’essai Discovery, une autre sous-étude de Solidarity4,15,16. Cela pourrait avoir des conséquences importantes pour les patients et pour les systèmes de santé, particulièrement lorsque les capacités en matière d’USI, de ventilation mécanique ou d’oxygénothérapie sont limitées.
Les conclusions de l’essai CATCO sont également importantes et complètent celles de Solidarity, car elles aident à répondre aux questions concernant l’applicabilité à grande échelle d’un protocole simple, déployé dans de nombreux hôpitaux et systèmes de soins de santé de pays à revenu faible et élevé. Le Canada est doté d’un système bien développé et relativement riche en ressources, avec un système de soins aigus et des soins intensifs sous réglementation fédérale et administration provinciale17. Les hospitalisations, y compris le coût des médicaments, sont en général entièrement couvertes par les provinces et le fédéral, avec des frais minimes, voire nuls, pour les patients. Le nombre de lits de soins aigus et de soins intensifs, même s’il a diminué au fil des ans, reste semblable à ceux de nombreux pays à revenu élevé18,19. Par conséquent, comprendre la variabilité des résultats entre les différents systèmes de santé est crucial lorsqu’il est question des bienfaits relatifs des médicaments qui pourraient procurer des avantages légers, mais réels.
L’essai CATCO a aussi permis de recueillir des données plus détaillées sur les patients recrutés comparativement à beaucoup d’autres régions dans le monde (p. ex., un suivi plus long de la mortalité et l’intégration des indicateurs d’innocuité); il propose des résultats applicables à d’autres systèmes de santé similaires. De même, l’essai CATCO a permis de continuer le recrutement de patients canadiens après la date d’arrêt de l’essai international, ajoutant 330 patients de plus qui ne faisaient partie de Solidarity, pendant une bonne partie de la troisième vague de COVID-19 au Canada et l’émergence du variant Alpha. Il s’agit du plus volumineux essai émanant d’un pays individuel sur le remdésivir publié à ce jour. Nous avons pu inclure les données de plusieurs ethnicités, une composante importante pour assurer la généralisabilité de nos résultats dans le système de santé canadien, ce qui rappelle l’utilité de recruter à partir d’un plus vaste bassin d’établissements de soins de santé15,20.
Les prises de décision relatives à l’utilisation du remdésivir au Canada bénéficieront de l’examen continu en économie de la santé, qui comparera les effets et les coûts potentiels du traitement par remdésivir au cours de cet essai. Les données de petits ERC sur l’équivalence des cycles de traitement de 5 ou de 10 jours devraient entrer en ligne de compte pour toute recommandation sur son déploiement21. Étant donné la forte probabilité d’un effet hétérogène du traitement par remdésivir selon la gravité de la maladie chez les patients hospitalisés, il sera important d’en assurer une gouvernance soigneuse.
Il sera aussi très important de comprendre les différences de risques entre les populations et les essais ainsi que l’incidence de ces derniers sur le rôle du remdésivir. La mortalité dans le groupe témoin de l’essai CATCO pour ce qui est du décès à 60 jours était de 28,2 %, c. 15,2 % pour la cohorte ACTT-1 à 29 jours16. Cela témoigne probablement de la phase de la pandémie où les patients ont été recrutés, de la gravité de la maladie au départ et de l’intérêt plus grand pour un recrutement dans les USI, pour la mortalité posthospitalière22, et peut-être, pour les contraintes imposées aux ressources hospitalières23. Les synthèses de données à venir entre les essais devraient tenir compte de ces risques différents au départ, en tant que modificateurs potentiels de l’effet.
Limites de l’étude
Ce rapport porte sur un nombre moindre de patients que l’essai principal Solidarity et est donc doté d’une puissance moindre pour montrer de manière indépendante la portée statistique de l’indicateur principal de mortalité. L’essai canadien représente les indicateurs d’une intervention offerte par un système de santé riche en ressources. Nos conclusions aident à comprendre les effets attendus dans des systèmes similaires; nos données concordent davantage avec celles de l’essai ACTT-1.
L’information sur le variant du SRAS-CoV-2 en cause n’était pas disponible à l’échelle des patients individuels; l’effet du remdésivir en tant qu’antiviral est donc impossible à évaluer pour différentes souches. Par contre, les patients de la troisième vague mentionnés ici ont fort probablement contracté la souche Alpha24. Comme la pandémie a évolué rapidement, il est important de mesurer l’incidence de l’évolution des soins pendant cet essai; des analyses chronologiques seront envisagées lors du traitement post hoc des données. Les indicateurs, comme le recours à la ventilation mécanique, subiront aussi l’influence des objectifs de soins pour les patients et nous ne pouvons écarter certains écarts entre les groupes en ce qui concerne l’admissibilité à la ventilation mécanique. Un indicateur mixte composé du recours à l’intubation et de la mortalité chez les patients non ventilés au départ pour l’analyse post hoc est inclus à l’annexe 1, au tableau S3.
Il a souvent été difficile durant la pandémie d’effectuer des suivis; ainsi, nous avons été incapables de contacter une partie des patients pour évaluer certains indicateurs après leur congé hospitalier.
En terminant, comme d’autres études de grande envergure sur cette pandémie, nous n’avons pas recueilli de données précises sur le dépistage dans les sites participants en raison des contraintes imposées aux systèmes de santé par la pandémie25. Étant donné le petit nombre de critères d’exclusion, il est peu probable que ces derniers aient une incidence négative sur la généralisabilité de nos observations, et le profil démographique des patients inscrits était similaire à celui de l’ensemble des patients canadiens hospitalisés pour la COVID-1926,27.
Conclusion
Cet essai a révélé que, comparativement au traitement standard seulement, chez les patients canadiens hospitalisés pour la COVID-19, le remdésivir en association avec le traitement standard a amélioré les indicateurs secondaires comme le recours à la ventilation mécanique chez les patients non ventilés au départ, même s’il n’était pas doté d’une puissance statistique suffisante pour détecter les différences de mortalité. Pour comprendre quelles populations de patients en bénéficieraient le plus, il faudra procéder à des méta-analyses.
Remerciements
Cet essai a bénéficié de l’appui généreux des Instituts de recherche en santé du Canada, de l’Institut de recherche Vancouver Coastal Health, du Centre d’essais et de recherche Northern Alberta Clinical, du Centre de recherche Covenant Health, de l’Initiative interdisciplinaire en infection et immunité McGill, de la fondation St. Joseph’s Health Care et de la fondation London Health Sciences. Les auteurs remercient Mark Duffett pour l’examen critique de ce manuscrit, et les pairs-réviseurs du JAMC qui ont grandement amélioré ce rapport.
Footnotes
↵* Auteurs: Karim Ali, Tanweer Azher, Mahin Baqi, Alexandra Binnie, Sergio Borgia, François M. Carrier, Yiorgos Alexandros Cavayas, Nicolas Chagnon, Matthew P. Cheng, John Conly, Cecilia Costiniuk, Peter Daley, Nick Daneman, Josh Douglas, Catarina Downey, Erick Duan, Emmanuelle Duceppe, Madeleine Durand, Shane English, George Farjou, Evradiki Fera, Patricia Fontela, Rob Fowler, Michael Fralick, Anna Geagea, Jennifer Grant, Luke B. Harrison, Thomas Havey, Holly Hoang, Lauren E. Kelly, Yoav Keynan, Kosar Khwaja, Gail Klein, Marina Klein, Christophe Kolan, Nadine Kronfli, François Lamontagne, Michael Lau, Todd C. Lee, Nelson Lee, Rachel Lim, Sarah Longo, Alexandra Lostun, Erika MacIntyre, Isabelle Malhamé, Kathryn Mangoff, Marlee McGuinty, Sonya Mergler, Matthew Munan, Srinivas Murthy, Conar O’Neil, Daniel Ovakim, Jesse Papenburg, Ken Kuljit S. Parhar, Seema Nair Parvathy, Chandni Patel, Santiago Perez-Patrigeon, Ruxandra Pinto, Subitha Rajakumaran, Asgar Rishu, Malaika Roba-Oshin, Moira Rushton, Mariam Saleem, Marina Salvadori, Kim Scherr, Kevin Schwartz, Makeda Semret, Michael Silverman, Ameeta Singh, Wendy Sligl, Stephanie Smith, Ranjani Somayaji, Darrell H.S. Tan, Siobhan Tobin, Meaghan Todd, Tuong-Vi Tran, Alain Tremblay, Jennifer Tsang, Alexis Turgeon, Erik Vakil, Jason Weatherald, Cedric Yansouni, Ryan Zarychanski.
Intérêts concurrents: Alexandra Binnie signale avoir reçu des subventions de recherche des Instituts de recherche en santé du Canada (IRSC) et de la fondation Physicians Services Incorporated. Sergio Borgia signale avoir reçu des honoraires des sociétés Gilead Sciences et GSK. Yiorgos Alexandros Cavayas signale avoir reçu une subvention des IRSC. Matthew Cheng signale avoir reçu des subventions de l’Initiative interdisciplinaire en infection et immunité McGill et des IRSC pendant la conduite de l’étude (paiements versés à l’établissement). Le Dr Cheng signale aussi avoir reçu des honoraires personnels d’AstraZeneca, indépendamment des travaux soumis et de Nplex Biosciences et GEn1E Lifesciences (sous forme d’options d’achat d’actions en tant que membre du comité consultatif scientifique) indépendamment des travaux soumis. Le Dr Cheng a cofondé Kanvas Biosciences et détient des participations dans la société; il a 3 demandes de brevets en instance. John Conly signale avoir reçu des subventions des IRSC, et de Pfizer, l’Organisation mondiale de la santé (OMS), l’Institut de recherche Sunnybrook, l’Université de Calgary et la fondation Calgary Health. Le Dr Conly signale aussi avoir reçu une aide pour participer à l’événement Think Tank Meeting 2019. Le Dr Conly est membre et président du Groupe d’experts de l’OMS pour la recherche et le développement des mesures de prévention et de contrôle des infections (PCI) pour la COVID-19, membre du groupe ad hoc de l’OMS pour l’élaboration des directives de PCI contre la COVID-19 du Programme de gestion des situations d’urgence sanitaire et membre du Groupe Cochrane pour les infections respiratoires aiguës. Madeleine Durand signale avoir reçu des subventions des IRSC et du Fonds de recherche Québec–Santé (FRQS). Rob Fowler signale avoir reçu une subvention des IRSC pour l’essai CATCO et il est détenteur de la chaire professorale H. Barrie Fairley en soins intensifs du Réseau universitaire de santé. Michael Fralick signale avoir reçu plusieurs subventions des IRSC et des subventions des Forces armées canadiennes pour des essais cliniques visant à identifier des traitements pour la COVID-19 (paiements versés à l’établissement). Le Dr Fralick est rémunéré à titre de consultant pour une entreprise en démarrage dénommée Proof DiagnosticsDx, qui a créé un dispositif clinique pour des tests de COVID-19 par technique CRISPR. Holly Hoang signale avoir reçu de CATCO Sunnybrook des sommes pour un poste d’assistanat de recherche (paiement versé à l’établissement) et une subvention de recherche du Centre de recherche en santé Covenant. Marina Klein signale avoir reçu des subventions des sociétés Gilead, ViiV Healthcare, Merck et AbbVie pour des études menées à l’initiative de chercheurs et des honoraires de consultation de Gilead, ViiV Healthcare, Merck et AbbVie, tous indépendamment des travaux soumis. Todd Lee signale avoir reçu des subventions de fonctionnement des IRSC et de l’Initiative interdisciplinaire en infection et immunité de McGill (MI4), et une bourse salariale du FRQS. Alexandra Lostun signale avoir reçu un financement par participant pour couvrir les frais de recrutement des patients (versé à l’établissement, Hôpital général de North York). François Carrier signale avoir reçu des subventions des lnstituts de recherche en santé du Canada et du Programme de recherche en don et transplantation du Canada, ainsi qu’une subvention et une bourse salariale du FRQS. Marlee McGuinty signale avoir reçu des honoraires de conférencière de Merck. Srinivas Murthy signale avoir reçu une subvention des IRSC, pendant la conduite de l’étude, il est la Chaire de recherche sur la préparation aux pandémies de la Fondation pour la recherche en santé de Médicaments novateurs Canada. Conar O’Neil signale avoir reçu une commandite pour une conférence de Gilead Sciences et il est membre d’un comité consultatif scientifique de Gilead. Jesse Papenburg signale avoir reçu une subvention des IRSC, pendant la conduite de l’étude, ainsi que des subventions de recherche et des contrats d’AbbVie et des contrats de recherche (investigateur pour un site d’essai clinique) de MedImmune, Merck et Sanofi Pasteur. Le Dr Papenburg a reçu des honoraires de consultation de Merck pour une réunion ad hoc d’un comité consultatif et des honoraires de présentateur de Seegene, AbbVie et AstraZeneca. Le Dr Papenburg est également membre ayant droit de vote du Comité consultatif national de l’immunisation. Ken Kuljit S. Parhar signale avoir reçu une subvention Projet des IRSC, une bourse d’Alberta Innovates et une bourse Application et Déploiement d’Alberta Health Innovation (versées à l’établissement). Seema Nair Parvathy signale avoir reçu du financement de la Fondation de l’Hôpital Saint-Joseph et de la fondation London Health Sciences. Moira Rushton-Marovac signale avoir reçu des honoraires comme membre d’un comité consultatif de Gilead. Marina Salvadori est une employée de l’Agence de la santé publique du Canada. Makeda Semret signale avoir reçu un soutien de McGill MI4 pour la plateforme de recherche clinique du Centre universitaire de santé qui a appuyé l’essai CATCO. Ameeta Singh signale avoir reçu des honoraires de consultation de Gilead à titre de membre d’un comité consultatif. Ranjani Somayaji signale avoir reçu des subventions de recherche contractuelle de l’Institut de recherche Sunnybrook, de l’Université de Calgary et de la fondation Calgary Health, et des subventions de recherche clinique des IRSC et de la Fondation de la fibrose kystique. Le Dr Somayaji signale aussi avoir fait partie du comité de surveillance de la sécurité des données sur l’oncovir. Darrell Tan signale avoir reçu des subventions d’AbbVie (en nature seulement) et de Gilead (en nature et sous forme de subventions versées à l’établissement) et l’existence d’un contrat entre GSK et son établissement pour des essais cliniques. Alain Tremblay signale avoir reçu des subventions de recherche contractuelle de l’Institut de recherche Sunnybrook et des subventions pour des essais cliniques sur la COVID-19 de l’Université de Calgary et de la fondation Calgary Health. Alexis Turgeon signale avoir reçu une subvention des IRSC. Jason Weatherald signale avoir reçu des subventions (versées à l’établissement) et des honoraires de consultation (personnels) de Janssen et d’Actelion, de même que des honoraires et une bourse de déplacement de Janssen. Le Dr Weatherald a fait partie de comités consultatifs de Janssen et Acceleron (rémunéré) et d’un comité de surveillance de la sécurité des données pour l’Université Laval (non rémunéré). Le Dr Weatherald signale aussi être membre du comité consultatif médical de la Pulmonary Hypertension Association of Canada et il est actionnaire de Precision Lung Consultants and Diagnostics. Cedric Yansouni signale avoir reçu des subventions du FRQS et des honoraires de consultation de Medicago Inc. Le Dr Yansouni signale aussi faire partie du comité indépendant de surveillance des données de Medicago Inc. et il a été conseiller scientifique du Groupe de travail sur l’immunité face à la COVID-19. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Réseau de recherche clinique de l’Association pour la microbiologie médicale et l’infectiologie (AMMI) Canada et Groupe canadien de recherche en soins intensifs: Barbara Antuna-Puente, Eneko Arhanchiague, Pascale Arlotto, Zeeshan Aslam, Fiona Auld, David Bellemare, Isaac Bogoch, Vikas Chaubey, Ève Cloutier, William Connors, Olivier Costerousse, Giulio DiDiodato, Charlene Fell, Greg Gamble, Stephen Giilck, Galo Ginocchio, Stephanie Go, Christopher Graham, Kaveri Gupta, Brent Guy, Amila Heendeniya, Susan John, Christopher Kandel, Anthony Ladelfa, François Lellouche, Allison Mah, Karen Mandelzweig, Sanjay Manocha, Caitlyn Marek, Rosa Myrna Marticorena, Stephanie Matte, Marc Messier-Peet, Patrick Mitchell, Elliott Owen, Elizabeth Parfitt, Lisa Patterson, Shaqil Peermohamed, Germain Poirier, Susan M. Poutanen, Jeff Powis, Natasha Press, Valerie Sales, Maureen Taylor.
Partage des données: Toutes les données individuelles des participants recueillies durant l’essai seront accessibles aux groupes externes, après anonymisation, à la suite de l’examen scientifique. Les propositions doivent être soumises à catco{at}sunnybrook.ca.
- Accepted December 20, 2021.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/