En Çok Okunanlar
Özet
Şiddetli akut solunum sendromu virusu (SARS-CoV-2)’nun neden olduğu koronavirus hastalığı 2019 (COVID-19), dünyayı etkilemiş, önemli morbidite ve mortalite nedeni olmuştur. COVID-19, esas olarak pulmoner belirtilerle ortaya çıkar, ancak vakaların yarısından fazlasında diğer organlarda özellikle hepatik tutulum gözlenir. Kronik hepatit C (KHC) dünya çapında önemli bir halk sağlığı sorunudur. Son yıllarda kullanıma giren doğrudan etkili antiviral (DEA) tedavilerle yüksek kalıcı virolojik yanıt (KVY) elde edilebilmekte ve HCV’ye bağlı gelişebilecek mortalite ve morbidite önlenebilmektedir. Ancak KHC’de tanı konulmazsa siroz ve karaciğer kanserine neden olabilir. Bu hastaların tanı ve tedavisi aralıklı takip gerektirdiğinden, pandemi sürecinden en çok etkilenen kronik hastalıklar arasındadır. COVID-19 pandemisinin ne zaman sonlanacağını kestirmek, pandeminin güncel koşullarında mümkün görünmemektedir. Sağlık kuruluşlarında korunma tedbirlerinin alındığı özel alanlarda KHC hastalarının tanı ve tedavi ihtiyaçları giderilebilmelidir. DEA tedavi başlanan hastalarda, tedavi takiplerinin mümkün olduğu ölçüde pandemi hizmeti vermeyen sağlık kuruluşlarınca yapılması sağlanmalı, gerekirse telefon iletişimine başvurulmalıdır.
GİRİŞ
Koronavirus hastalığı 2019 (COVID-19) ağır akut solunum sendromu virusu-2 (SARS-CoV-2)’nin neden olduğu bir infeksiyondur. Dünya Sağlık Örgütü (DSÖ) tarafından 11 Mart 2020 tarihinde pandemi ilan edilmiştir ve halen yaşamın tüm alanlarında dünyayı etkilemeye devam etmektedir (1). COVID-19 pandemisinin etkilerinin ve yayılımının daha ne kadar süreceği konusunda belirgin bir öngörü yoktur. Pandemi nedeniyle tüm dünyada özellikle kronik hastalıkları olan kişiler hem COVID-19 hem de kronik hastalıklarının yönetimi açısından ciddi risk taşımaktadır (2). Bu hastalıklardan birisi de kronik hepatit C (KHC) infeksiyonudur. Parenteral yolla bulaşan, hastaların büyük kısmında asemptomatik seyreden, ancak tanı almazsa siroz ve karaciğer kanserine neden olabilen, hastaların tanı ve tedavisi için aralıklı takip gerektiren KHC, bu özellikleri nedeniyle pandemi sürecinden en çok etkilenen kronik hastalıklar arasındadır (3). Diğer kronik hastalıklarda olduğu gibi KHC’de de pandemi döneminde hasta izlemleriyle ilgili önemli sorunlar yaşanmıştır. Pandemi döneminde KHC infeksiyonu tedavisini değerlendirmeden önce güncel KHC yönetimini vurgulamak uygun olacaktır.
GÜNCEL KRONİK HEPATİT C TEDAVİSİ
KHC dünya çapında önemli bir halk sağlığı sorunudur. DSÖ’nün son verilerine göre dünya genelinde 71 milyon kişi hepatit C virusu (HCV) ile kronik olarak infektedir. Son yıllarda kullanıma giren doğrudan etkili antiviral (DEA) tedavilerle yüksek kalıcı virolojik yanıt (KVY) elde edilebilmekte ve HCV’ye bağlı gelişebilecek mortalite ve morbidite önlenebilmektedir (4). KVY elde edilen hastaların %99’undan fazlası HCV infeksiyonundan tamamen kurtulur.
KHC tedavisi 1996 yılında interferon (İFN) ile başlamış ve bu alanda geliştirilen tedavi rejimleriyle KVY oranında önemli artış sağlanmıştır (5). Günümüzde tüm HCV genotiplerine etkili, iyi tolere edilebilen, kısa tedavi süresi olan ve kolay kullanılabilen DEA ajanların kullanıma girmesiyle tedavideki başarı oranı artmıştır. Günde tek veya üç tabletlik pangenotipik ve RBV içermeyen rejimlerle %95 veya daha yüksek kür oranları elde edilmektedir (6).
Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği Viral Hepatit Çalışma Grubu tarafından 2017 yılında güncellenen KHC infeksiyonunun yönetimi başlıklı uzlaşı raporunda HCV genotip 1 ile infekte hastaların tedavisinde SOF / ledipasvir (LDV), paritaprevir (PTV)/ritonavir (RTV)/ombitasvir (OBV)+dasabuvir (DSV), SOF/velpatasvir (VEL), grazoprevir (GRZ)/elbasvir (EBV), SOF+daclatasvir (DCV), SOF+simeprevir (SMV) kombinasyonları önerilmiştir (7). HCV genotip 4 ile infekte hastalarda PTV’li kombinasyon tedavisinde DSV olamaması dışında aynı tedavi seçenekleri yer almaktadır. HCV genotip 2 ve 3 ile infekte hastalarda SOF/LDV, SOF/DCV, HCV genotip 5 ve 6 ile infekte olgularda ise SOF/LDV, SOF/VEL ve SOF/DCV önerilen tedavi seçenekleridir.
Pangenotipik seçenekler olarak glecaprevir (GLE)/pibrentasvir (PIB) ve SOF/VEL/voxilaprevir (VOX) kombinasyonlarının klinik kullanıma sunulmasının ardından güncel tedavi kılavuzlarında bu seçenekler yer almıştır. Amerika Karaciğer Hastalıkları Derneği ve Amerika İnfeksiyon Hastalıkları Derneği tarafından hazırlanan kılavuzda naif veya peg-İFN+RBV deneyimli sirotik olmayan veya kompanse sirotik hastalarda genotiplere göre önerilen tedavi şemaları aşağıda özetlenmiştir (8):
HCV genotip 1a/1b infeksiyonu:
- GZR (100 mg)/EBR (50 mg) – 12 hafta (GT1a’da elbasvire bazal direnç yoksa, GT1b ile infekte naif-sirotik olmayan hastalarda fibroz hafifse 8 hafta verilebilir.)
- GLE/PIB – 8 hafta (Deneyimli sirotik hastalarda 12 hafta)
- SOF/LDV (90 mg) – 12 hafta (HIV koinfeksiyonu olmayan, HCV RNA<6 milyon İÜ/ml, naif-sirotik olmayan hastalarda 8 hafta verilebilir. Deneyimli-sirotik hastalarda alternatif tedavide RBV ile kombine kullanılabilir.)
- SOF/VEL (100 mg) – 12 hafta
CV genotip 2 infeksiyonu:
- GLE/PIB – 8 hafta (Deneyimli-sirotik hastalarda 12 hafta)
- SOF/VEL – 12 hafta
HCV genotip 3 infeksiyonu:
- GLE/PIB – 8 hafta (Deneyimli-sirotik olmayan [alternatif tedavi] ve olan hastalarda 16 hafta)
- SOF/VEL – 12 hafta (Deneyimli-sirotik olmayan, naif veya deneyimli-sirotik hastalarda VEL’e karşı NS5A RAS Y93H mutasyonu yoksa kullanılır. Sirotik hastalarda mutasyon varsa ve deneyimli-sirotik hastalarda RBV ile kombine olarak uygulanabilir [naif ve deneyimli-sirotik hastalarda alternatif].)
- SOF/VEL/VOX – 12 hafta (NS5A RAS Y93H mutasyonu olan, naif-sirotik hastalarda ve deneyimli-sirotik olmayan hastalarda alternatif tedavide kullanılabilir.)
- GZR/EBR – 12 hafta (Deneyimli-sirotik hastalarda alternatif)
- GZR + SOF – 12 hafta (Deneyimli-sirotik hastalarda alternatif)
HCV genotip 4 infeksiyonu
- GLE/PIB – 8 hafta (Deneyimli-sirotik hastalarda 12 hafta)
- SOF/LDV – 12 hafta (Deneyimli-sirotik hastalarda RBV ile kombine alternatif tedavi)
- SOF/VEL- 12 hafta
- GZR/EBR – 12 hafta (Deneyimli-sirotik olan veya olmayan relaps hastalarında )
HCV genotip 5/6 infeksiyonu
- GLE/PIB- 8 hafta (Deneyimli-sirotik hastalarda 12 hafta)
- SOF/VEL – 12 hafta
- SOF/LDV – 12 hafta (Naif GT6e’de önerilmez.)
Avrupa Karaciğer Araştırmaları Derneği (European Association for the Study of the Liver – EASL) 2018 kılavuzunda da benzer öneriler yer almakla beraber en dikkat çekici fark genotip 1b ile infekte hastalarda PTV-RTV/OBV+DSV kombinasyon tedavisinin önerilmesidir (9). Ek olarak bu kılavuzda RBV içeren kombinasyonların nadir durumlar dışında önerilmemesidir. Amerikan Karaciğer Hastalıkları Araştırma Derneği (American Association for the Study of Liver Diseases-AASLD) ve Amerika İnfeksiyon Hastalıkları Derneği (Infectious Diseases Society of America-IDSA) 2020 yılında güncellediği kılavuzda ise tedavi-naif, sirotik olan ve olmayan hastalar için GLE/PIB – 8 hafta ve SOF/VEL- 12 hafta (sirotik hastalarda HCV genotip 1,2, 4, 5 ve 6 için) kombinasyonları önerilmektedir (10).
Ülkemizde 04.09.2019 tarihli Sağlık Uygulama Tebliği (SUT)’ne göre GLE/PIB kombinasyonu naif, sirotik olmayan hastalara 8 hafta süreyle ve Child-Pugh sınıflamasına göre A grubunda olan, kompanse sirotik hastalara ise 12 hafta süreyle önerilmektedir (11). Daha önce Peg-İFN, Peg-İFN+RBV, Peg-İFN+RBV+BOC/TLV kullanmış, NS5A deneyimsiz, sirotik olmayan HCV genotip 3 dışı infeksiyonu olan hastalarda GLE/PIB 8 hafta süreyle, NS5A deneyimi varsa 16 hafta süreyle önerilmektedir. Child-Pugh sınıflamasına göre A grubunda olan, kompanse sirotik hastalarda NS5A deneyimi yoksa 12 hafta, varsa 16 hafta önerilmektedir. HCV genotip 3 ile infekte NS5A-naif veya deneyimli hastalarda tedavi süresi 16 hafta olarak bildirilmiştir. Child-Pugh sınıflamasına göre B ve C grubunda olan, HCV genotip 1, 4, 5 ve 6 ile infekte naif veya deneyimli (Peg-İFN, Peg-İFN+RBV, Peg-İFN+RBV+BOC/TLV deneyimi olan) hastalara, NS5A deneyimi olsun veya olmasın SOF/LDV+RBV kombinasyonu 12 hafta süreyle önerilmiştir. PTV-RTV/OBV+DSV kombinasyonu HCV genotip 1a ile infekte, naif veya NS5A dışı deneyimli, sirotik olmayan hastalara RBV ile kombine 12 hafta, sirotik hastalara 24 hafta süreyle verilmektedir. HCV genotip 1b ile infekte naif, sirotik olmayan veya kompanse sirotik hastalarda 8 veya 12 hafta önerilmektedir. NS5A dışı deneyimi olanlarda ise 12 hafta süreyle verilmesi önerilmiştir. HCV genotip 4 ile infekte naif veya deneyimli (NS5A-naif olanlarda) kompanse sirotik olan veya olmayan hastalarda PTV-RTV/OBV+RBV tedavisi 12 hafta süreyle önerilmektedir. SUT’ta 16.06.2020 tarihinde yapılan son güncellemeyle daha önce DEA kullanan ancak başarı elde edilmemiş hastalara ikinci kez DEA tedavi kullanma seçeneği ortaya çıkmıştır (12).
Ülkemizde DEA tedavilerin sonuçlarıyla ilgili gerçek yaşam verileri yayımlanmıştır. HCV genotip 1 ve 4 ile infekte, naif veya İFN bazlı tedavi deneyimi olan 862 hastada PTV-RTV/OBV±DSV±RBV kombinasyon tedavisinin sonuçlarının değerlendirildiği araştırmada KVY12 oranı %99.1 (sirotik olmayan hastalarda %99.5, kompanse sirotik hastalarda %95.5) bulunmuştur (13).
KHC tedavisinde DEA ilaç çağıyla kür elde edilebiliyor olması, DSÖ tarafından tüm dünyada HCV eliminasyonuna yönelik bir planlama yapılmasının önünü açmıştır. Global hepatit eliminasyonunu hedefleyen DSÖ’nün bu programının uygulanmasında sorunlar yaşanmazsa, 2015 yılından 2030 yılına kadar HCV olgu sayısının %90 azalarak 170 binlere inmesi, yine HCV’yle ilişkili ölümlerin de %65 azalarak 140 bine inmesi öngörülmektedir (14). Tüm dünyada HCV eliminasyonuna yönelik planlama ve çalışmalar yapılırken ortaya çıkan COVID-19 pandemisi yürütülmekte olan süreçlerin belirgin şekilde aksamasına neden olmuştur (4,2).
COVID-19 PANDEMİSİ
Pandemi döneminde EASL ve Avrupa Klinik Mikrobiyoloji ve Enfeksiyon Hastalıkları Derneği (European Society of Clinical Microbiology and Infectious Diseases-ESCMID)’in karaciğer hastalığı olan hastaların bakımına ilişkin açıklamalarında bu bakımın yerel ve/veya ulusal infeksiyon dinamikleri ve politikalarıyla karaciğer hastalığının şiddeti arasında dengeleyici olması gerektiği bildirilmiştir. COVID-19 ve karaciğere etkisi hakkında cevaplanmamış sorular bulunmaktadır. Viral kinetik ve hepatobiliyer/gastrointestinal yolaklar arasındaki ilişki, immünosüpresyonun COVID-19 seyrine etkisi ve virusun indüklediği hepatik dekompansasyon riski bu sorulardan bazılarıdır (15).
Bu hastalar açısından iki temel sorun bulunmaktadır. Bu problemlerden ilki tedavi başlanması gereken hastaların tedavilerinin başlanamaması sonucu hastalık progresyonu (siroz, hepatoselüler kanser; HSK, karaciğer yetmezliği) riski olması, ikincisi ise tedavi almakta olan hastaların tedavilerinin yarım kalması veya kesintiye uğramasıdır (16,17). Mevcut sorunların doğru yönetilmesi için COVID-19 hastalarında karaciğerdeki değişimlerin bilinmesi önemlidir.
COVID-19 VE KARACİĞER
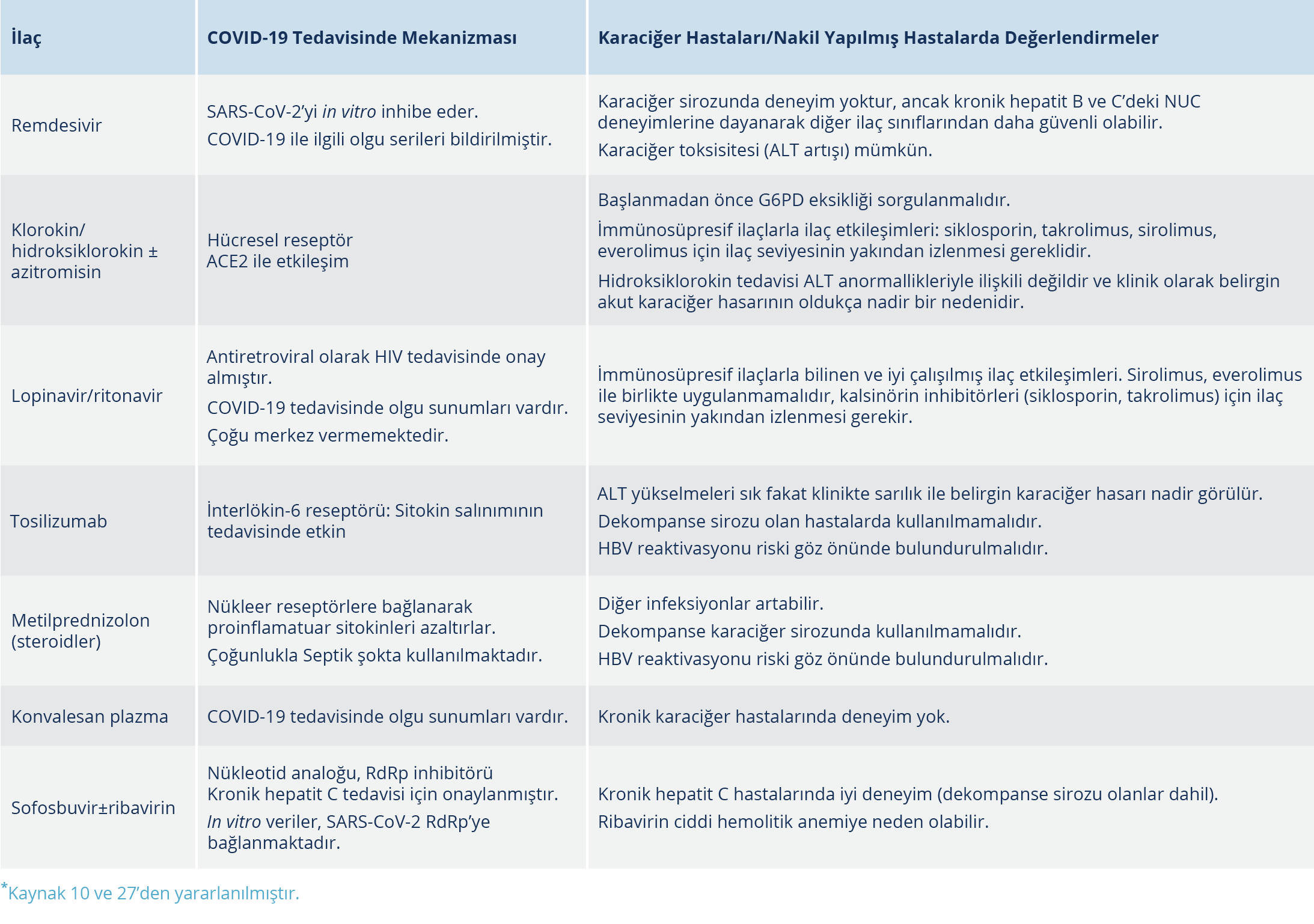
Tablo 1. COVID-19 Tedavisi için Önerilen/Tartışılan İlaçlar ve Karaciğer Hastalığı Olan veya Karaciğer Nakli Yapılmış Hastalar için Değerlendirmeler*
COVID-19, asıl olarak akciğer bulgularıyla ortaya çıksa da olguların yarısından fazlasında diğer organlar, özellikle de karaciğer tutulumları izlenmektedir (18,19). Mevcut çalışmalarda hastaların %14.8-%53’ünde anormal aspartat aminotransferaz (AST)/alanin aminotransaminaz. (ALT) düzeylerine eşlik eden hafif bilirübin yüksekliğiyle ortaya çıkan karaciğer hasarı olduğu bildirilmektedir. Mortal seyreden hastalarda ise bu oran %78’e kadar çıkabilmektedir (20). Şu ana kadar yayımlanan kohort çalışmalarında, önceden var olan kronik karaciğer hastalıkları ayrıntılı olarak bildirilmemiş olsa da yüksek ALT seviyeleri, düşük trombosit sayısı ve albümin seviyesi hastalarda yüksek mortaliteyle ilişkilendirilmiştir (21). Olgu serilerinde ALT ve AST düzeylerinin normal üst sınırın üç katından fazla olmayacak şekilde arttığı, serum bilirübin düzeyi artan hasta oranının %10 civarında olduğu, hastaların %50 kadarında da GGT serum düzeyinin arttığı belirtilmektedir (21-23).
Mortalite gelişen COVID19 hastalarının karaciğer biyopsi örneklerinde orta düzeyde hepatosteatoz ve hafif lobuler/portal aktivite olduğu bildirilmektedir (24). COVID-19 hastalarında klinik olarak görülen hepatobiliyer patolojilerin ve karaciğer histolojisindeki değişikliklerin olası nedenleri şu şekilde özetlenebilir (24,25):
- Hepatik hücrelerde SARS-CoV-2’nin aktif replikasyonu ve direkt sitopatik etkisi
- COVID-19 infeksiyonuna bağlı gelişen komplikasyonlar veya tedavileri
- Virusun neden olduğu ağır inflamasyona bağlı değişiklikler, sepsis, septik şok, hipoksik hasar ve/veya ventilatör komplikasyonları
- İlaçlar (antibiyotikler, antiviraller veya destek amaçlı kullanılan diğer ilaçlar) (Tablo 1’de COVID-19 tedavisi için önerilen/tartışılan ilaçlar ve karaciğer hastalığı olan veya karaciğer nakli yapılmış hastalar için değerlendirmeler yer almaktadır.)
- Daha önce tanı konul(a)mamış altta yatan karaciğer hastalıkları (HAV, HBV, HCV, HEV, alkole bağlı karaciğer hastalığı, otoimmün karaciğer hastalığı vb.)
COVID-19 VE KARACİĞER HASTALIĞININ/KHC’NİN YÖNETİMİ
EASL ve ESCMID’in açıklamasında EASL-COVID-HEP (Avrupa) ve SECURE-CIRRHOSIS (Amerika-Asya) ile birlikte yapılan iki büyük kayıt çalışmasında ulaşılan ilk bulgulara göre COVID-19 gelişen sirotik hastalarda, nonsirotik veya posttransplant hastalara göre daha yüksek mortalite ve morbidite olduğu gösterilmiştir (17).
Pandemi dönemi ve sonrasında muhtemel ikinci bir karaciğerle ilişkili morbidite ve mortalite dalgası olacağı öngörülmektedir. Bu dönemde hastaların tedaviye erişimi ve tanısal yaklaşımlarda önemli aksamalar olmuştur (18). COVID-19’un viral hepatit bakımına etkisini değerlendirmek için Dünya Hepatit Birliği (World Hepatitis Alliance – WHA)’nın araştırmasında 32 ülkede hasta anketi yapılmış, sonuçlar ve gözlemler sunulmuştur. Buna göre, COVID-19 pandemisi hastaların viral hepatit tedavisine erişimini etkilemiştir. Bu anket sonuçlarına göre viral hepatiti olan hastaların %30’u tedaviye erişememektedir. COVID-19 ile temas korkusu hareket, seyahat veya servislerin kapatılmasından daha büyük bir engel olarak görülmektedir. Katılımcıların çoğu viral hepatitle yaşayan insanlar için ülkelerinde COVID-19 hakkında yeterli bilgi sağlanmadığını düşünmektedir (26).
COVID-19’un karaciğer hastalarının bakımı üzerine etkisinde ülke deneyimlerine bakıldığında; yeniden düzenleme ve yeniden önceliklendirme nedeniyle hizmete ulaşılabilirlikte önemli azalma, HCV taramalarında azalma, uzamış laboratuvar test süreçleri, HCV tedavisi başlanmasında azalma, bazı ortamlarda sınırlı tedaviye ulaşım ve hastane dışı COVID-19 harici morbidite artışı en sık rastlanan sorunlardır (16).
AASLD kılavuzuna göre, yeni teşhis edilen KHC vakalarında SARS-CoV-2 infeksiyonu yoksa ve kaynaklar yeterliyse (örneğin eczane hizmetleri, tedavinin onaylanması için personel, kan testi hizmeti, tele-sağlık veya yüz yüze takip tesisleri) antiviral tedavi başlanabileceği belirtilmiştir. Yaşanan pandemi sürecinde sağlık kurumlarındaki kaynakların etkin kullanılması çok önemlidir. Dolayısıyla rehberde, mevcut ekip, ekipman ve diğer kaynakların COVID-19 faaliyetleri için konuşlandırılmış olması gerekliliği vurgulanmaktadır. Aynı rehberde, yakın zamanda teşhis edilmiş bir HCV infeksiyonuyla birlikte COVID-19 tanısı konulmuş olanlar için koronavirus infeksiyonu tedavisi tamamlanana kadar HCV tedavisinin ertelenmesi önerilmektedir. Yine HCV tedavisine yönelik DEA almakta olan ve COVID-19 tanısı alanların tedavisine, yakın takiple devam edilebileceği belirtilmektedir (27).
COVID-19 salgınının ilk günlerinden itibaren rehberlerde genel olarak önerilen, hepatit C veya siroz +/- HSK ile yaşayan tüm bireylerin tedavi ve bakımının optimize edilmesi ve düzenlenmesi şeklindedir. Avustralya Gastroenteroloji Derneğinin (Gastroenterological Society of Australia-GESA) önerilerine göre (Gastroenterological Society of Australia, GESA) pandemi döneminde KHC hastalarında DEA tedavisine başlanmalıdır (28).
Güncel tedavi rehberlerinde KHC tanısı almış tüm hastalara tedavi önerilmekle birlikte, METAVIR skoru F 0-2 evresinde olan ve ekstrahepatik bulguları olmayan hastalarda tedavinin geciktirilebileceği bilinmektedir (7). Eğer salgın nedeniyle klinik hizmetler kısıtlı ve olanaklar yetersizse bu grupta tedavi ertelenebilir. KHC nedeniyle DEA ilaç tedavisi başlanmış hastalarda ise, hastaların büyük kısmında ilaçlar önemli bir yan etkiye neden olmadığı ve hızlı klinik yanıt alındığı için, tedavinin devam ettiği 8-12 haftalık dönemde klinik takibe gerek olmayabilir. Ancak bu dönemde tedaviye uyum sorunu ve HCV reinfeksiyonu olasılıklarının dışlanması için, hastanede takip yerine aile hekimi yardımı ya da telefon görüşmeleriyle hasta takibi yöntemlerine başvurulabilir (29).
KHC hastaları arasında METAVIR skoru F3/4 evresinde olan hastalar, dekompanse sirozu olanlar, HIV ve HBV koinfeksiyonu olanlar, karaciğer transplantasyonu indikasyonu olanlar ve karaciğer transplantasyonundan sonra HCV infeksiyonu rekürans gösterenler tedavi için öncelikli gruptur (7). Bu grup hastaların pandemi koşullarında da tedaviye ulaşması gerekir. Ancak bu hastaların tedavi sürecinde, HSK için sürveyans, ultrasonografi vb. görüntülemeleri, kamu hastanelerinde yapılıyorsa, bunların güvenli alanlarda yapılmaları için sağlık kurumlarında özel alanların ayrılması, radyoloji uygulamalarının güvenli ortamlarda yapılmalarının sağlanması gereklidir. Bu hastalarda sık görülen özofagus varislerinin bantlanması için gastroskopiler gerektiğinde, rutin olarak ertelenmemelidir. Bununla birlikte, SARS-CoV-2 bulaşmasının yüksek riski nedeniyle bu hizmetlere erişim gittikçe sınırlanmaktadır ve bir gastroenterolog/hepatolog ile görüşme vaka bazında önerilmektedir (29).
KHC tedavisinde kullanılan güncel DEA ilaçlar gebelerde kontrindikedir. Gebelik planı olan KHC’li kadınların gebelik öncesinde tedavi alması gerekir. Bu grup da, KHC tedavisinde öncelikli hastalar arasında yer almaktadır (10). Pandeminin ne zaman sonuçlanacağı belli olmadığı için, rehber önerisinden yola çıkılarak, pandemi nedeniyle gebelik planlayan kadın KHC hastalarının tedavileri de ertelenmemelidir. COVID-19’dan korunmak için alınması gereken önlemlere maksimum uyum sağlayarak tedavi planlamaları yapılmalıdır. Ancak COVID-19 tanısı alan, kronik HCV’li hamile kadınlarla ilgili erken dönem yapılan olgu bildirimlerinde anne ölümü görülmediği ve hastalığının klinik özelliklerinin ve sonuçlarının hamile olmayan kadınlardan farklı olmadığı da bildirilmektedir (30,31). Mevcut kanıtlar, 50 yaşın altındaki kişilerin ve kadınların COVID-19 infeksiyonundan ciddi sonuçlara sahip olma olasılığının daha düşük olduğunu göstermektedir, ancak hamile kadınların spesifik durumunu bildirmek için daha fazla veri beklenmektedir (31).
COVID-19 pandemisinin ne zaman sonlanacağını kestirmek, pandeminin güncel koşullarında mümkün görünmemektedir. Hastalığın kür sağlayacak tedavisi ne yazık ki henüz geliştirilmiş değildir. Tüm bu nedenlerle, pandemi varlığı süresince kronik hastalık tanı ve tedavilerinin ertelenmesi çok rasyonel bir yaklaşım gibi görünmemektedir. Bu bağlamda KHC hastalarının da tanı ve tedavisi asgari düzeyde sürdürülmeli, özellikle öncelikli tedavi alması gereken KHC hasta grubunda, tedavi ötelenmemelidir. Sağlık kuruluşlarında korunma tedbirlerinin alındığı özel alanlarda KHC hastalarının tanı ve tedavi ihtiyaçları giderilebilmelidir. DEA tedavi başlanan hastalarda, tedavi takiplerinin mümkün olduğu ölçüde pandemi hizmeti vermeyen sağlık kuruluşlarınca yapılması sağlanmalı, gerekirse telefon iletişimine başvurulmalıdır. Ancak COVID-19 korunma tedbirleri çerçevesinde, tedavisi geciktirilebilecek KHC hastalarının beklemeye alınabileceği de göz önünde bulundurulmalıdır.
Çıkar çatışması
Yazarlar, herhangi bir çıkar çatışması bildirmemiştir.
Referanslar
- World Health Organization. WHO Director-General’s opening remarks at the media briefing on COVID-19- 11 March 2020 [İnternet]. Geneva: WHO [erişim 28 Mart 2020]. https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19—11-march-2020.
- Centers for Disease Control and Prevention. What to Know About Liver Disease and COVID-19 (Updated May 5, 2020) [İnternet]. Atlanta: CDC [erişim 28 Haziran 2020]. https://www.cdc.gov/coronavirus/2019-ncov/need-extra-precautions/liver-disease.html.
- Cortez KJ, Kottilil S. Beyond interferon: rationale and prospects for newer treatment paradigms for chronic hepatitis C. Ther Adv Chronic Dis. 2015; 6(1): 4-14.
- World Health Organization. Chronic Hepatitis C Global Report (Updated July 9, 2019). Geneva: WHO [erişim 28 Haziran 2020]. https://www.who.int/news-room/fact-sheets/detail/hepatitis-c.
- Aygen B, Yildiz O, Akhan S, et al. Impact of interleukin 28B genotype on the virological responses in chronic hepatitis C treatment. Gastroenterology Res. 2014; 7(5-6): 123-30.
- Falade-Nwulia O, Suarez-Cuervo C, Nelson DR, Fried MW, Segal JB, Sulkowski MS. Oral direct-acting agent therapy for hepatitis C virus infection: A systematic review. Ann Intern Med. 2017; 166(9): 637-48.
- Aygen B, Demirtürk N, Türker N, et al. Kronik hepatit C virusu infeksiyonunun yönetimi: Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği Viral Hepatit Çalışma Grubu Uzlaşı Raporu-2017 Güncellemesi. Klimik Derg. 2017; 30 (Suppl. 1): 2-36.
- American Association for the Study of Liver Diseases and Infectious Diseases Society of America. HCV guidance: recommendations for testing, managing, and treating hepatitis C, last updated November 6, 2019, [İnternet]. Alexandria and Arlington, VA: AASLD and IDSA [erişim 1 Temmuz 2020]. https://www.hcvguidelines.org/.
- European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C 2018. J Hepatol. 2018; 69(2): 461-511.
- Ghany MG, Morgan TR; AASLD-IDSA Hepatitis C Guidance Panel. Hepatitis C Guidance 2019 Update: American Association for the Study of Liver Diseases-Infectious Diseases Society of America Recommendations for Testing, Managing, and Treating Hepatitis C Virus Infection. Hepatology. 2020; 71(2): 686-721.
- Sosyal Güvenlik Kurumu. Sağlık Uygulama Tebliğinde Değişiklik Yapılmasına Dair Tebliğ. Resmi Gazete. Sayı 30878 (Mükerrer), 4 Eylül 2019.
- Sosyal Güvenlik Kurumu. Sağlık Uygulama Tebliğinde Değişiklik Yapılmasına Dair Tebliğ. Resmi Gazete. Sayı 31157 (Mükerrer), 16 Haziran 2020.
- Aygen B, Demirtürk N, Yıldız O, et al. Real-world efficacy, safety, and clinical outcomes of ombitasvir/paritaprevir/ritonavir ± dasabuvir ± ribavirin combination therapy in patients with hepatitis C virus genotype 1 or 4 infection: The Turkey experience experience. Turk J Gastroenterol. 2020; 31(4): 305-17.
- WHO. Global hepatitis report 2017 [İnternet]. Geneva: World Health Organization [erişim 10 Temmuz 2020]. https://www.who.int/hepatitis/publications/global-hepatitis-report2017/en/.
- Boettler T, Newsome PN, Mondelli MU, et al. Care of patients with liver disease during the COVID-19 pandemic: EASL-ESCMID position paper. JHEP Rep. 2020; 2(3): 100113.
- Tapper EB, Asrani SK. The COVID-19 pandemic will have a long-lasting impact on the quality of cirrhosis care. J Hepatol. 2020; 73(2): 441-5.
- EASL. COVID-Hep Registry [İnternet] Geneva, Switzerland: The European Association for the Study of the Liver [erişim 10 Temmuz 2020]. https://easl.eu/easl-covid-hep-registry/.
- Bangash MN, Patel J, Parekh D. COVID-19 and the liver: little cause for concern. Lancet Gastroenterol Hepatol. 2020; 5(6): 529-530.
- Zhang C, Shi L, Wang FS. Liver injury in COVID-19: Management and challenges. Lancet Gastroenterol Hepatol. 2020; 5(5): 428-30.
- Xu L, Liu J, Lu M, Yang D, Zheng X. Liver injury during highly pathogenic human coronavirus infections. Liver Int. 2020; 40(5): 998-1004.
- Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020; 395(10229): 1054-62.
- Fan Z, Chen L, Li J, et al. Clinical features of COVID-19-related liver functional abnormality. Clin Gastroenterol Hepatol. 2020; 18(7): 1561-6.
- Guan WJ, Ni ZY, Hu Y, et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020; 382(18): 1708-20.
- Sun J, Aghemo A, Forner A, Valenti L. COVID-19 and liver disease. Liver Int. 2020; 40(6): 1278-81.
- WGO. Guidance for Patients with COVID-19 and Liver Disease [İnternet]. Milwaukee, WI: World Gastroenterology Organisation [erişim 1 Temmuz 2020]. https://www.worldgastroenterology.org/publications/e-wgn/wgo-guidance-for-patients-with-covid-19-and-liver-disease.
- World Hepatitis Alliance. Latest News [İnternet]. London, UK: World Hepatitis Alliance [erişim 18 Haziran 2020]. https://www.worldhepatitisalliance.org/latest-news.
- Fix OK, Hameed B, Fontana RJ, et al. Clinical best practice advice for hepatology and liver transplant providers during the COVID-19 pandemic: AASLD expert panel consensus statement. Hepatology. 2020; 72(1): 287-304.
- PBS. General Statement for Drugs for the Treatment of Hepatitis C [İnternet]. Canberra, Australia: Department of Health Pharmaceutical Benefits Scheme [erişim 25 Haziran 2020]. http://www.pbs.gov.au/healthpro/explanatory-notes/generalstatement-pdf/general-statement-hepatitis-c.pdf.
- Hepatitis C Virus Infection Consensus Statement Working Group. Australian recommendations for the management of hepatitis C virus infection: a consensus statement (September 2018) [İnternet]. Melbourne: Gastroenterological Society of Australia, 2018 [erişim 10 Temmuz 2020]. https://research.monash.edu/en/publications/australian-recommendations-for-the-management-of-hepatitis-c-viru.
- Schwartz DA. An analysis of 38 pregnant women with COVID-19, their newborn infants, and maternal-fetal transmission of SARS-CoV-2: Maternal coronavirus infections and pregnancy outcomes. Arch Pathol Lab Med. 2020; (Baskıda).
- Yu N, Li W, Kang Q, et al. Clinical features and obstetric and neonatal outcomes of pregnant patients with COVID-19 in Wuhan, China: A retrospective, single-centre, descriptive study. Lancet Infect Dis. 2020; 20(5): 559-64.





























































































































