Zusammenfassung
Die Global Initiative for Asthma (GINA) hat in den Jahren 2019–2021 einige substanzielle Änderungen für das Management von Patienten mit Asthma empfohlen, die auch Schulkinder und Jugendliche betreffen. Eine sehr wesentliche neue Empfehlung ist, dass kurzwirksame Betamimetika (SABA) aus Sicherheitsgründen nur mehr in Kombination mit inhalativen Steroiden (ICS) gegeben werden sollten. Bei Jugendlichen werden GINA-Stufe 1 und 2 zusammengezogen und bei Asthmaproblemen eine Bedarfsinhalation mit niedrig dosierter ICS-Formoterol-Kombination empfohlen. Als Alternative wird die Trennung in Stufe 1 mit Inhalation von SABA und einem ICS bei Bedarf und in Stufe 2 wie bisher die tägliche Inhalation eines ICS und SABA bei Bedarf empfohlen. Dieser Weg wird auch als der bevorzugte bei Kindern von 6 bis 11 Jahren vorgeschlagen. Diese neuen GINA-Empfehlungen wurden jedoch nicht von allen nationalen oder internationalen Leitlinien übernommen, da vor allem für Kinder die Evidenz dafür gering ist. Tiotropium, Mepolizumab und Dupilumab wurden in die Therapie des schweren Asthmas aufgenommen.
Kinder mit Asthma erkranken nicht häufiger oder schwerer an COVID-19 als Kinder ohne Asthma. Verschiedene Mechanismen wie ein möglich protektiver Effekt der Typ-2-Inflammation, die antivirale und immunmodulierende Wirkung von ICS und die Niederregulierung von ACE2-Rezeptoren durch die allergische Sensibilisierung könnten dafür verantwortlich sein.
Abstract
In the years 2019–2021, the Global Initiative for Asthma (GINA) recommended some fundamental changes in the management of patients with asthma, that also affect school children and adolescents. A very significant new recommendation is that for safety, short-acting β2-agonists (SABA) should now be given in combination with inhaled corticosteroids (ICS). In adolescents, GINA steps 1 and 2 are combined and a low-dose ICS formoterol combination as needed is recommended for asthma problems. Alternatively, separation into step 1, with inhalation of SABA and an ICS as needed, and step 2, with daily inhalation of an ICS and SABA as needed, as before, is recommended. This path is suggested as the preferred treatment in children aged 6–11 years. However, these recommendations have not been adopted by all national and international guidelines, because the evidence is weak, especially in children. Tiotropium, mepolizumab, and dupilumab were added to the therapy for severe asthma.
Children with asthma do not become ill with COVD-19 more often or more severely than children without asthma. Various mechanisms, such as a possible protective effect of type 2 inflammation, the antiviral and immunomodulatory effects of ICS, and the downregulation of ACE2 receptors by allergic sensitization could be responsible for this.
Similar content being viewed by others
Explore related subjects
Discover the latest articles and news from researchers in related subjects, suggested using machine learning.Avoid common mistakes on your manuscript.
Das Ziel der vorliegenden Publikation ist die Darstellung der wichtigsten Neuerungen, die die Global Initiative for Asthma (GINA) im Management des Kindes mit Asthma empfiehlt. GINA gibt keine Leitlinien, sondern jährliche Expertenempfehlungen heraus (www.ginasthma.org). Diese Empfehlungen sollen auf Populationsebene weltweite Wirkung haben und sind nicht immer kompatibel mit länderspezifischen Leitlinien oder behördlichen Zulassungen von Therapien im Asthmamanagement. Im zweiten Teil der Arbeit wird auf die Auswirkungen von COVID-19 auf Kinder mit Asthma eingegangen.
Pathophysiologie
In der Phänotypisierung des kindlichen Asthmas geht GINA aktuell auf die 2 verschiedenen Endotypen Typ-2-Asthma und Non-Typ-2-Asthma (oder Typ-2-Asthma low) ein. Diese Differenzierung ist vor allem als klinisch behandelbares Charakteristikum („treatable trait“) von Bedeutung. Beim Typ-2-Asthma sind sowohl im Blut als auch im induzierten Sputum die eosinophilen Zellen erhöht, während beim Non-Typ-2-Asthma neutrophile Zellen überwiegen oder eine paucigranulozytäre Zellverteilung vorliegt. Die dominanten Zellen des Typ-2-Asthmas sind Th2-Zellen, „innate lymphoid cells 2“ (ILC2), natürliche Killerzellen und Mastzellen, während beim Non-Typ-2-Asthma Th1- und Th17-Zellen überwiegen. Die entsprechenden Zytokine sind bei ersterem IL3, IL4, IL5, IL9, IL13 und Periostin, bei letzterem IF‑γ, IL17, IL22, IL23 und IL8.
Therapie des milden Asthmas
Die fundamentalste Änderung im Asthmamanagement wurde von GINA bereits 2019 vorgeschlagen [1, 2]. Aus Sicherheitsgründen empfiehlt GINA die alleinige Verwendung von kurzwirksamen Betamimetika (SABA) nicht mehr. Diese Sicherheitsbedenken stammen in erster Linie aus Untersuchungen an Erwachsenen mit Asthma, bei denen eine schlechte Adhärenz mit der empfohlenen inhalativen Steroidtherapie (ICS), ein ungerechtfertigt hoher SABA-Verbrauch und ein damit einhergehendes erhöhtes Asthmaexazerbationsrisiko gefunden wurde [3]. Die Autoren folgern, dass vor allem bei Erwachsenen zu viele Patienten mit Asthma auf die Kurzzeitwirkung des SABA vertrauen und ihre Symptome zu lange ausschließlich damit behandeln, was aufgrund der fehlenden antiinflammatorischen Wirkung zu vermehrten Exazerbationen führen kann. Eine Verwendung von 3 oder mehr SABA-Dosieraerosolen pro Jahr (entspricht z. B. mindestens 600 Hüben Salbutamol) erhöht das Risiko, eine Asthmaexazerbation zu erleiden, um 26 % [3]. Eine so hohe Anzahl von jährlichen SABA-Inhalationen wird wohl bei Kindern und Jugendlichen kaum oder nie erreicht werden.
Unterstützt wurde diese Empfehlung von 2 großen Studien im Jahr 2018 bei Erwachsenen und einem Anteil von Jugendlichen von 9,9 und 12,5 % der untersuchten Population mit mildem persistierendem Asthma (GINA-Stufe 2), bei denen ein Vorteil der Bedarfstherapie mit ICS plus Formoterol gegenüber einer alleinigen SABA-Therapie gezeigt wurde [4] und dass die Bedarfs-ICS plus Formoterol-Therapie nicht schlechter abschnitt als eine tägliche Langzeittherapie mit ICS [5]. Dies traf jedoch nur auf die Anzahl der Exazerbationen, nicht jedoch auf andere Parameter wie Lungenfunktion, Symptomenkontrolle und Lebensqualität zu.
In der Folge gab es sehr viel Kritik an dieser Empfehlung, weil Daten zu GINA-Stufe 2 auf GINA-Stufe 1 ohne Evidenz übertragen wurden [6]. Daraufhin definierte GINA das milde Asthma neu, empfiehlt jetzt keine Trennung mehr zwischen episodischem (GINA-Stufe 1) und mild persistierendem (GINA-Stufe 2) Asthma und zieht bei Erwachsenen und Jugendlichen Stufe 1 und 2 zusammen. GINA hält fest, dass in den verschiedenen Stufen nicht unterschiedliche Phänotypen oder Schweregrade abgebildet werden sollten, sondern notwendige Therapiemaßnahmen zur Symptomenkontrolle und zur Reduktion von Exazerbationen des Asthmas [7]. Daher wird als Track 1 in Therapiestufe 1 und 2 bei Erwachsenen und Jugendlichen ab 12 Jahren eine Bedarfstherapie von niedrig dosiertem ICS plus Formoterol als bevorzugter „controller“ empfohlen. Das Betamimetikum soll in allen Therapiestufen als „reliever“ nicht mehr allein, sondern auch als ICS plus Formoterol gegeben werden (Abb. 1). Dies wird empfohlen, wenn Asthmasymptome an weniger als 4–5 Tagen pro Woche auftreten (eine Häufigkeit von Symptomen, die bei Kindern und Jugendlichen eindeutig einem persistierenden Asthma entspricht und bei der in allen Leitlinien zum kindlichen Asthma eine tägliche ICS-Therapie und keine alleinige SABA-Therapie empfohlen wird; [8]).
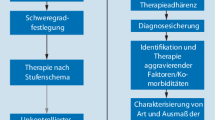
GINA-Stufenplan der Asthmatherapie bei Jugendlichen. (GINA© 2021 Global Initiative for Asthma, reprinted with permission. Available from www.ginasthma.org)
Der Alternativweg Track 2 trennt weiterhin Therapiestufe 1 (Symptome seltener als zweimal pro Monat) und Stufe 2 (Symptome zweimal oder häufiger pro Monat aber seltener als an 4–5 Tagen der Woche) und empfiehlt in Stufe 1 als „preferred controller“ bei Gabe eines SABA zusätzlich ein ICS (welches auch immer). In Stufe 2 wird eine Erhaltungstherapie mit täglichem ICS und SABA bei Bedarf vorgeschlagen. Dieser Track 2 soll bei jenen Patienten angewandt werden, die wenig oder keine Exazerbationen haben und wird auch bei Kindern zwischen 6 und 11 Jahren empfohlen (Abb. 2). Für Kinder unter 5 Jahren wird in Stufe 1 kein „preferred controller“ und alleiniges SABA als „reliever“ empfohlen. Stufe 2 ist identisch für Kinder zwischen 6 und 11 Jahren (Abb. 3).
GINA-Stufenplan der Asthmatherapie bei 6‑ bis 11-jährigen Kindern. (GINA© 2021 Global Initiative for Asthma, reprinted with permission. Available from www.ginasthma.org)
GINA-Stufenplan der Asthmatherapie bei Vorschulkindern. (GINA© 2021 Global Initiative for Asthma, reprinted with permission. Available from www.ginasthma.org)
Da diese neuen Empfehlungen besonders für Kinder und Jugendliche unter Umständen nicht für alle Populationen gleich geeignet sind, haben sich mehrere Fachgesellschaften in Österreich, Deutschland und der Schweiz zusammengeschlossen und Ende 2020 ein Addendum zur 2017 erstellten DACH-Leitlinie für die Diagnose und die Therapie des Asthmas ausgearbeitet [8].
Ich zitiere aus diesem Addendum 2020: „Im Unterschied zu Erwachsenen werden bei Kindern und Jugendlichen deutlich weniger Symptome akzeptiert, um das Asthma als kontrolliert einzustufen. Eine bedarfsorientierte Inhalation eines kurzwirksamen inhalativen Beta-2-Sympathomimetikums (SABA) reicht zur Symptomkontrolle aus. Treten häufigere oder regelmäßige Beschwerden auf, ist eine Dauertherapie mit niedrigdosierten ICS indiziert, da diese das Risiko schwerer Asthmaexazerbationen, des Abfalls der Lungenfunktion und des Kontrollverlustes reduzieren können [7]. Bei Jugendlichen (nicht jedoch bei Kindern) gibt es Hinweise, dass eine Bedarfstherapie mit einer Fixkombination aus einem ICS und Formoterol (ICS/Formoterol-Fixkombination) die Wahrscheinlichkeit reduziert, mittelschwere bis schwere Asthma-Exazerbationen zu erleiden [4, 5].“
Diese sehr aktuelle mitteleuropäische Leitlinie für das Asthma bei Kindern und Jugendlichen unterscheidet sich daher in mehreren Punkten von den GINA-Empfehlungen, was ja durchaus verständlich ist, da GINA damit in erster Linie eine weltweit gültige „population-level risk reduction strategy“ verfolgt, während länderspezifische Leitlinien auf die lokalen Gegebenheiten mehr Rücksicht nehmen.
In Ergänzung zu diesen wissenschaftlichen Fakten und Überlegungen müssen auch Aspekte der Anwendung der verschiedenen Inhalationsgeräte besonders bei Kindern berücksichtigt werden, worauf GINA nicht explizit eingeht. Der Turbohaler (für die empfohlene ICS-/Formoterol-Fixkombination) war eines der ersten Geräte zur Inhalation von Trockenpulver und verfügt noch nicht über hilfreiche Feedbacksignale (optisch, olfaktorisch und akustisch) zur individuellen Überprüfung der Inhalationstechnik wie dies in moderneren Inhalationsgeräten der Fall ist. Zudem ist der zu einer optimalen intrabronchialen Teilchengrößendeposition notwendige inspiratorische Spitzenfluss von 60 l/min sehr hoch und wird von vielen Kindern vor allem bei einer Atemwegsobstruktion nicht erreicht. Die Bedarfs-ICS-plus-Formoterol-Therapie (mittels Turbohaler) ist bei Kindern unter 12 Jahren in Österreich nicht zugelassen.
GINA empfiehlt in Stufe 2 bei 6‑ bis 11-jährigen Kindern Leukotrienrezeptorantagonisten (LTRA) als „controller options“, während die österreichischen Kinderpneumologen aufgrund des aktuellen „blackbox warning“ der FDA bezüglich beunruhigender neurologischer und psychiatrischer Nebenwirkungen eine sehr restriktive Haltung zu LTRA einnehmen [9].
Therapie des schweren Asthmas
An einem schweren Asthma leiden 1–3 % der Kinder mit Asthma. Mehrere Studien zeigten, dass inhalatives Tiotropiumbromid, ein langwirksames Anticholinergikum, als Add-on-Therapie zu hochdosierten ICS (GINA Stufe 5) zu einer signifikanten Zunahme des FEV1 führen kann [10]. In Österreich ist Tiotropium aktuell ausschließlich als Spiriva® Respimat (Boehringer Ingelheim, Deutschland) ab 6 Jahren für schweres Asthma zugelassen.
Mepolizumab und Reslizumab, 2 Anti-IL5-Antikörper, sowie Benralizumab, ein Anti-IL5-Rezeptor-Antikörper, sind intensiv in der Therapie des schweren unkontrollierten Asthmas mit Eosinophilie als Add-on-Therapie untersucht worden und Mepolizumab ist für Kinder und Jugendliche ab 6 Jahren in dieser Indikation zugelassen. Der Anti-IL4-Rezeptor-Antikörper (blockiert den Signalweg für IL4 und IL13) Dupilumab ist für schweres refraktäres Typ-2-Asthma des Erwachsenen und Jugendlichen ab 12 Jahre als Add-on-Therapie zugelassen. Bei Asthmapatienten, die eine Langzeittherapie mit einem oralen Glukokortikoid hatten, wurde durch die Gabe von Dupilumab als Add-on-Therapie die Glukokortikoiddosis um 70 % reduziert [11].
Sowohl in GINA 2019/2020 als auch in der länderübergreifenden aktuellen S2-k-DACH-Leitlinie [12] finden sich erstmals – allerdings etwas unterschiedliche – Empfehlungen für den Einsatz der spezifischen Immuntherapie beim Asthma des Kindes.
Therapie des Non-Typ-2-Asthmas
In der Therapie des Non-Typ-2-Asthmas hat sich wenig geändert. Die Verabreichung eines Anti-IL17-Antikörpers (Brodalumab) zeigte keinen Effekt bei Erwachsenen mit unkontrolliertem moderaten oder schweren Asthma. Die Gabe von Makroliden als Add-on-Therapie zu ICS und LABA bewirkte bei einer Subgruppe von erwachsenen Patienten mit nichteosinophilem Asthma eine signifikante Reduktion der Asthmaexazerbationen. Azithromycin wurde auch zur Therapie des Asthmas im Vorschulalter untersucht. Dabei zeigte eine Studie eine Reduktion der Tage mit Atemwegsobstruktion um 63 % [13] und eine zweite Studie fand eine signifikante Verringerung der Progression einer obstruktiven Bronchitis zu einer schweren Infektion [14]. Aufgrund der Sorge möglicher Nebenwirkungen wie QT-Verlängerung, Ototoxizität und vor allem der potenziellen Zunahme der Makrolidresistenzen kann eine allgemein gültige Empfehlung für die Verwendung von Makroliden bei rezidivierenden obstruktiven Bronchitiden oder dem Asthma bei Kindern nicht gegeben werden [15].
Auswirkungen von COVID-19 auf Kinder mit Asthma
Als im März 2020 der erste Lockdown wegen der Zunahme von SARS-CoV-2-Infektionen in Österreich ausgesprochen wurde, war die Sorge von Patienten mit Asthma groß, schwerer oder häufiger an COVID-19 zu erkranken als atemwegsgesunde Menschen. Eltern von Kindern mit Asthma waren besonders verunsichert. Bald hat sich jedoch herausgestellt, dass diese Sorgen unberechtigt sind. In Österreichs Kinder- und Jugendabteilungen kam es zu keinen vermehrten stationären oder ambulanten Vorstellungen wegen Asthmaproblemen (regelmäßige Umfrage der AG Infektiologie der Österreichischen Gesellschaft für Kinder- und Jugendheilkunde [ÖGKJ]). In einer europäischen Umfrage an 174 Asthmabetreuungszentren wurde kein erhöhtes Risiko für Kinder mit Asthma und SARS-CoV-2-Infektion gefunden (im Unterschied zu Kindern mit bronchopulmonaler Dysplasie; [16]). Dies wurde auch in mehreren anderen Ländern der Welt bestätigt [17]. Kinder mit Asthma erkranken nicht häufiger oder schwerer an COVID-19 als Kinder ohne Asthma. In der Folge zeigten Untersuchungen, dass die COVID-19-Pandemie mit den entsprechenden Lockdowns zu einer Reduktion von stationären Aufnahmen und Notfallvorstellungen von Kindern und Jugendlichen mit Asthma führte [18]. Vielleicht konnten einige Asthmaattacken schon im Vorfeld durch die sich im Homeoffice befindlichen Betreuungspersonen ausreichend beherrscht werden. Es gibt jedoch auch Vermutungen und Hinweise, dass folgende Mechanismen dafür verantwortlich sein könnten [19]:
-
Das Tragen von Gesichtsmasken, das Abstandhalten und die Händedesinfektion reduzieren generell virale Infekte als Auslöser für Asthmaattacken
-
Die Medikamentenadhärenz, vor allem für ICS, steigt in der Pandemie aus Furcht vor COVID-19
-
Antivirale und immunmodulierende Rolle der ICS
-
Allergisches Asthma führt zu weniger IFN-α-Produktion und damit weniger Inflammation bei COVID-19
-
Protektive Rolle der eosinophilen Zellen
-
Allergische Sensibilisierung führt zur Downregulation von ACE2-Rezeptoren und damit weniger SARS-CoV-2-Viruseintritt in die Lunge
Es ist daher unsere Aufgabe als Kinderärztinnen und -ärzte, Eltern und Patienten mit Asthma bezüglich COVID-19 zu beruhigen, sie zur konsequenten Verwendung ihrer Medikamente zu motivieren und zur Teilnahme an den angebotenen SARS-CoV-2-Impfungen aufzufordern.
Fazit für die Praxis
-
Die zwei Endotypen Typ-2-Asthma und Non-Typ-2-Asthma sind behandelbare Charakteristika („treatable traits“).
-
Kurz wirksame Betamimetika (SABA) sollten aus Sicherheitsgründen zur Verhinderung möglicher Asthmaexazerbationen nicht ohne inhalative Steroide gegeben werden.
-
Bei Jugendlichen kann das ICS bei mildem Asthma auch als Bedarfstherapie mittels niedrig dosiertem ICS-Formoterol verwendet werden.
-
Bei Schul- und Vorschulkindern ist weiterhin die tägliche Inhalation von ICS und SABA bei Bedarf die Therapie der Wahl, wenn häufige Symptome bestehen.
-
Tiotropiumbromid und Mepolizumab können ab 6 Jahren, Dupilumab ab 12 Jahren als Add-on-Therapie beim schweren Asthma eingesetzt werden.
-
Makrolide können beim Non-Typ-2-Asthma nicht generell empfohlen werden.
-
Kinder mit Asthma erkranken nicht häufiger oder schwerer an COVID-19 als Kinder ohne Asthma.
Literatur
Global Initiative for Asthma (GINA) (2019) Global strategy for asthma management and prevention. http://ginasthma.org/. Zugegriffen: 15. Mai 2021
Reddel HK, FitzGerald JM, Bateman ED et al (2019) GINA 2019: a fundamental change in asthma management. Treatment of asthma with short-acting bronchodilators alone is no longer recommended for adults and adolescents. Eur Respir J 53:1901046
Nwaru BI, Ekström M, Hasvold P et al (2020) Overuse of short-acting β2-agonists in asthma is associated with increased risk of exacerbation and mortality: a nationwide cohort study of global SABINA programme. Eur Respir J 55:1901872
O’Byrne PM, FitzGerald JM, Bateman ED et al (2018) Inhaled combined budesonide-formoterol as needed in mild asthma. N Engl J Med 378:1865–1876
Bateman ED, Reddel H, O’Byrne PM et al (2018) As-needed budesonide-formoterol versus maintenance budesonide in mild asthma. N Engl J Med 378:1877–1887
Ferretti S, Gelsomino M, Miceli Sopo S (2021) About the recommendation of the GINA strategy report on asthma step 1. Eur Respir J 57:2003324
Reddel HK, Busse WW, Pedersen S et al (2017) Should recommendations about starting inhaled corticosteroid treatment for mild asthma be based on symptom frequency: a post-hoc analysis of the START study. Lancet 389:157–166
Buhl R, Bals R, Baur X, Berdel D, Criée CP, Gappa M, Gillissen A, Greulich T, Haidl P, Hamelmann E, Kardos P, Kenn K, Klimek L, Korn S, Lommatzsch M, Magnussen H, Nicolai T, Nowak D, Pfaar O, Rabe KF, Riedler J, Ritz T, Schultz K, Schuster A, Spindler T, Taube RC, Taube K, Vogelmeier C, von Leupold A, Wantke F, Weise S, Wildhaber J, Worth H, Zacharasiewicz A (2021) Guideline for the diagnosis and treatment of asthma—addendum 2020. Guideline of the German Respiratory Society and the German Atemwegsliga in cooperation with the Paediatric Respiratory Society and the Austrian Society of Pneumology. Pneumologie 75(3):191–200
Zschocke A, Zacharasiewicz A, Riedler J et al (2021) Stellungnahme der AG-Pneumologie und Allergologie der ÖGKJ zur FDA Warnung Montelukast 03.2020. Wien Klin Wochenschr. (eingereicht)
Hamelmann E, Szefler SJ (2018) Efficacy and safety of tiotropium in children and adolescents. Drugs 78:327–338
Rabe KF, Nair P, Brusselle G et al (2018) Efficacy and safety of dupilumab in glucocorticoid-dependent severe asthma. N Engl J Med 378:2475–2485
Buhl R, Bals R, Baur X, Berdel D, Criée CP, Gappa M, Gillissen A, Greulich T, Haidl P, Hamelmann E, Kardos P, Kenn K, Klimek L, Korn S, Lommatzsch M, Magnussen H, Nicolai T, Nowak D, Pfaar O, Rabe KF, Riedler J, Ritz T, Schultz K, Schuster A, Spindler T, Taube RC, Taube K, Vogelmeier C, von Leupold A, Wantke F, Weise S, Wildhaber J, Worth H, Zacharasiewicz A (2017) Guideline for the diagnosis and treatment of asthma—guideline of the German Respiratory Socciety and the German Atemwegsliga in cooperation with the Paediatric Respiratory Society and the Austrian Society of Pneumology. Pneumologie 71(12):849–919
Stokholm J, Chawes B, Vissing N et al (2016) Azithromycin for episodes with asthma-like symptoms in young children aged 1–3 years: a randomised, double-blind, placebo-controlled trial. Lancet Respir Med 4:19–26
Bacherier L, Guilbert T, Mauger D et al (2015) Early administration of azithromycin and prevention of severe lower respiratory tract illness in preschool children with a history of scuh illnesses: a randomised clinical trial. JAMA 314(19):2034–2044
Cohen R, Pelton S (2015) Individual benefit vs societal effect of antibiotic prescribing for preschool children with recurrent wheeze. JAMA 314(19):2027–2029
Möller A, Thanikkel L, Duijts E et al (2020) COVID-19 in children with underlying chronic respiratory diseases: survey results from 174 centres. ERJ Open Res 6(4):00409–2020
Gray DM, Davies MA, Githinji L et al (2021) COVID-19 and pediatric lung disease: a South African tertiary center experience. Front Pediatr 8:614076
Bover-Bauza C, Rossello Gomila MA, Perez DD et al (2021) The impact of the SARS-CoV‑2 pandemic on the emergency department and management of the pediatric asthmatic patient. J Asthma Allergy 14:101–108
Boechat JL, Wandalsen GF, Kuschnir FC et al (2021) COVID-19 and pediatric asthma: clinical and management challenges. Int J Environ Res Public Health 18(3):1093
Author information
Authors and Affiliations
Corresponding author
Ethics declarations
Interessenkonflikt
J. Riedler gibt an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Additional information
Hinweis des Verlags
Der Verlag bleibt in Hinblick auf geografische Zuordnungen und Gebietsbezeichnungen in veröffentlichten Karten und Institutsadressen neutral.
Rights and permissions
About this article
Cite this article
Riedler, J. Neuerungen durch GINA 2020 bei Kindern und die Auswirkungen von COVID-19 auf Kinder mit Asthma. Paediatr. Paedolog. 56, 152–159 (2021). https://doi.org/10.1007/s00608-021-00908-3
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/s00608-021-00908-3